本カテゴリー「論文紹介」では管理者の独断と偏見と気まぐれで選んだ論文を解説します.
論文は図表の貼り付けや結果の細かな紹介はできませんが、最小限の結果(abstractで公開されている範囲)を引用する形で紹介していきます。また、図表もそのまま貼り付けることはせず、オリジナルのイメージ図に替えて掲載致します.
主旨としては管理者自らの疫学・統計学・臨床医学上の個人的解釈とし、Stataのコード紹介なども行っていきます.内容の詳細がご覧になりたい場合にはぜひ本文を正式に入手してください.
なお、内容の是非に踏み込んだコメントも致しますが、本ブログは情報提供だけを目的としたもので、医学的アドバイス(診断、治療、予防)の代わりになるものではありません。また診療目的でのアドバイスやご質問も受け付けておりませんので宜しくお願いいたします.
さて、本日紹介する論文は、SGLT2阻害薬の腎保護効果のメカニズムを媒介効果で示したもの(Nephrol Dial Transplant 2024; 39: 1504-1513)です.似たような研究がcanagliflozin(Kidney int 2020)でも行われていますが、今回はEMPA-REG OUTCOME trialのpost hoc analysisです.
これら2つのStudyで採用されている方法を比較しながらStata的にどうやるのか?というようなことを考えてみたいと思います.ちなみに本文はOpen accessですので誰でも全文読むことができます.
糖尿病治療薬として知られるSGLT2阻害薬の腎保護効果が明らかになり、様々な機序が提唱されていますが、確定的なものはまだありません.
- Tubuloglomerular feedback (TGF)の活性化→糸球体内圧を下げる
- 近位尿細管での代謝ストレスや低酸素の軽減
- 高血糖誘発性の炎症・酸化的リン酸化・活性酸素種(ROS)の低減
- 溢水の解除
などが言われているようです.
先に述べた2つの研究結果から、どうやら赤血球造血に関するパラメータ(HbやHt)が媒介していそうだ、ということが明らかになりました.
1. Canagliflozinの媒介効果分析
2020年にcanagliflozinで行われた媒介効果分析は、ランダム化後の各種バイオマーカーの変化をCoxモデルに投入してHRの変化を見ています.具体的にはランダム化後の平均値、ランダム化後の早期変化、ランダム化後の変化(mixed-effects modelで推定)
媒介効果自体の計算は、以下のように
the percentage mediation was estimated as follows: 100%×{(HR – HRc)/(HR – 1)}, where HRc is the hazard ratio after adjustment for the biomarker and HR is the unadjusted hazard ratio. The 95% CIs for the estimated percentage mediation were obtained using a 5000-iteration bootstrap resampling procedure.
この方法は管理者も自分の論文で採用させてもらいましたが、査読者からこっぴどく絞られました….
Causal mediation analysisをやりなさい!と言われてRを使って解析をしてSupplementaryに結果を追加しました.
ちなみにそのときは欠測値の補完を行うMultiple imputationsとbootstrap resamplingを組み合わせる必要がありました.完全データ分析であればそのままbootstrapできるのですが、欠測値があるデータセットですのでそこは工夫が必要でした.
方法として
- BootMI: bootstrap resamplingのたびにmultiple imputationする
- MIboot: multiple imputationで生成されたデータセット一つ一つに対してbootstrapし、最終的にRubinのルールで結果を統合
のいずれを選択するのが良いのだろうか、と悩みました.参考にした文献によれば、どちらもよさそうでしたが、前者の方が計算量が多いことが挙げられていました.
Mの数が少ないときや、多重補完の安定性がいまいちなときには前者を選択することが勧められていましたが、20セットとまあ十分な数のデータセットを導出していたと考えたので、後者を行うことを選択しました.(これならStataでやれそう!という思いからですが…)
以下のようなプログラムを書いて実行しましたが、計算量少ないとはいえかなりの日数をかけて実行しました.
program myboot, rclass
syntax [if] [in]
stcox cov1 cov2 cov3 `if' `in'
local hr1 = exp(_b[exposure])
stcox mediator cov1 cov2 cov3 `if' `in'
local hr2 = exp(_b[exposure])
disp `hr1', `hr2'
return scalar opm = (`hr1' - `hr2')/(`hr1'-1)
end
forvalues n = 1/20 {
preserve
mi extract `n', clear
stset time_cnsr, id(subjid) failure(cnsr ==1)
bootstrap r(opm), reps(1000) seed(2112115) dots(1000): myboot
est store margin_`n'
restore
}
noi est tab margin_*, b(%7.6f) se(%7.6f)
noi mirubin, stub(margin_)さらにCausal mediation analysisでも実行しなさい!ときましたので、R package “CMAverse”
(https://bs1125.github.io/CMAverse/) を使って解析を追加しました.
方法の詳細に関しては論文のSupplementary methodsをご参照ください.Open accessですので誰でも読めます.
さて、ちなみにこの論文と同じ著者が心臓のアウトカムで似たような、というかほぼ同じ解析をしていますね(JACC HF 2020).一度で二度おいしいって感じでしょうか.ひとネタで大型のジャーナル2つですからいいですね.旬なネタだとそんなこともアリなんでしょうか.
論文の研究に話を戻しましょう.
この論文では赤血球造血がSGLT2阻害薬により一過性に促され、それによって組織低酸素状態が改善することで腎保護効果が得られているのではないか、と考察されていました.
SGLT2阻害薬によるMediatorである赤血球産生に対する強いAcute effectがよりその後の腎機能改善に効いていることを解析しての結果を受けているのかなと思います.
2.EMPA-REG OUTCOME研究のpost hoc研究
BaronとKellyによるtraditionalなmediation analysisに基づいて解析したと書かれています.満たすべき3つの条件として、
- 処置が時間経過を経てある変数に対して影響を与えたときにのみ媒介因子とする
- 時間を経て治療によって受けた変化が測定されたアウトカムに影響を持つことが必要である
- ハザード比によって表現される治療効果が、媒介因子を含むモデルにおいて減じる
ここまで見ればなんとなく基本のコンセプトは1の研究とそんなに違わなさそうです.
ですが、mediatorsをモデルの中でどのように扱うかについては違いがありそうです.
We analyzed the association of each of these variables as a time-dependent covariate with the composite kidney outcome (i.e. the second mediation condition) in Cox regression models using two approaches for the time-dependent covariate: (i) current change from baseline to the most recent value available before the first event of the composite kidney outcome (“current change”); (ii) mean value considering all prior values (“updated mean”). Analysis of the current change represents the current effect of the variable on the risk of the outcome. Analysis of the updated mean represents the cumulative effect of all prior values of the variable on the risk of the outcome.
これは時間とともに変化する媒介因子の扱い方を示しています.
- ベースラインからの差分をとって、それを時間依存変数としてCoxモデルに投入.current changeについて、短期的な効果を評価
- これまでのすべての値を平均化したものを時間依存性変数としてCoxモデルに投入.updated meanとして蓄積効果を評価
というようにやるようです.そしてunadjustedモデルと、これらの時間依存変数によるadjustedモデルとでHRを比較するというものです.
その評価の仕方は以下の式で表現しています.上記の論文とは若干異なるものの、大筋としては同じような感じです.こちらの論文に詳細は説明があります.
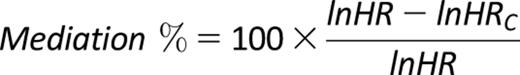
前者のcurrent changeデザインで、12週時点のtime-fixedとしたランドマークデザインで最終的な結果は表示しているようです.
As an alternate methodological approach, we performed “landmark” Cox regression analyses, wherein each of the variables was analyzed as a time-fixed covariate at Week 12 (using current change from baseline or updated mean), along with the variable baseline value as a covariate and a factor for treatment group.
ちなみに12週時点のtime-fixedデザインをメインにしていますが、time-dependentなcurrent changeモデルは感度分析としてサプリに回っています.
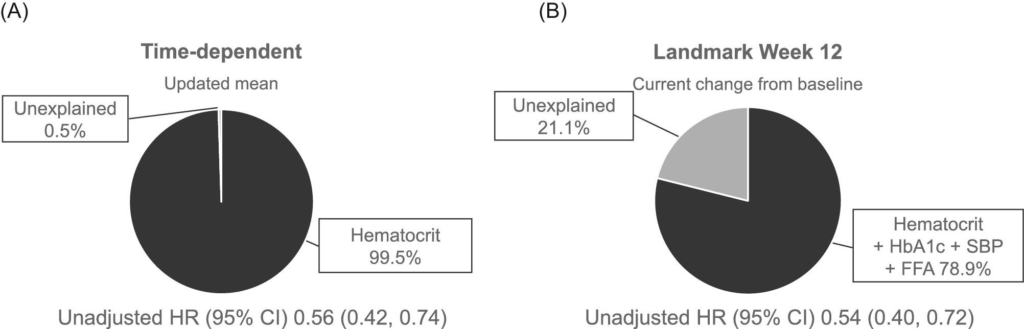
この結果をみると、蓄積効果の方が12週時点のcurrent changeの効果よりも媒介効果が強いという風に見えますので、以下のように解釈されていました.
the long-term impact of hematocrit and hemoglobin on the composite kidney outcomes appears to be stronger than the impact of the initial change up to Week 12. The initial changes may mainly reflect hemoconcentration from plasma volume reduction due to urinary sodium and water losses, whilst long-term changes likely represent mainly erythropoiesis via enhanced erythropoietin secretion by the kidney.
短期的な効果としては体液貯留の是正による血液濃縮の可能性を挙げていますが、それよりも長期効果が勝るということは本当に赤血球造血そのものが良い効果をもたらしてくれている可能性があるんだ、ということのようです.
まとめ
ということでいかがだったでしょうか?
媒介効果分析の基本的なプログラムの走らせ方はすでに別の記事で紹介していますが、実際に研究デザインに落とし込む際には結構しっかりと考えないといけませんね.
個人的には後者の方法がやりやすそうかな、という印象を受けました.



コメント